
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
BABIO sichert sich die 510(k)-Zulassung der US-amerikanischen FDA für sein Virus-Transport-Kit (nicht inaktivierend)
BABIO sichert sich die 510(k)-Zulassung der US-amerikanischen FDA für sein Virus-Transport-Kit (nicht inaktivierend)
Jinan, China – Oktober 2025 – Jinan Babio Biotechnology Co., Ltd. (BABIO)verkündet stolz, dass es so istBabio® Virus Transport Kit (nicht inaktivierend)offiziell erhalten hatFDA 510(k)-Zulassung (K250205). Diese Zertifizierung stellt einen wichtigen Meilenstein für BABIO dar und bekräftigt sein Engagement für globale Qualität, Sicherheit und Innovation in der klinischen Diagnostik und mikrobiologischen Transportsystemen.
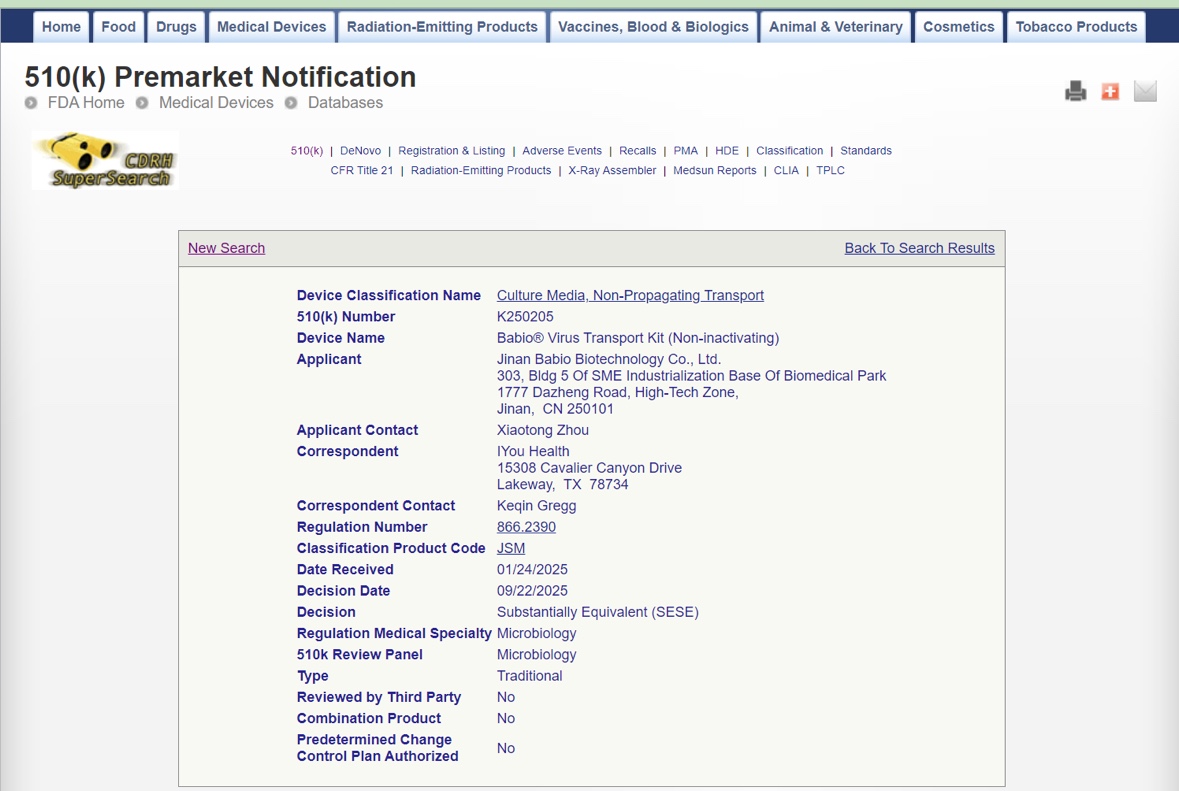
Mit der 510(k)-Zulassung der FDA ist das Babio® Virus Transport Kit zugelassenim Wesentlichen gleichwertigfür legal in den USA vermarktete Geräte und bestätigt die Einhaltung der US-amerikanischen Regulierungsstandards für Medizinprodukte. Dieser Erfolg demonstriert die starken F&E-Fähigkeiten und die hervorragende Fertigungsqualität von BABIO und stärkt seine globale Wettbewerbsfähigkeit in der Branche weiterMarkt für Virentransport und Probenentnahme.

DerBabio® Virus Transport Kit (nicht inaktivierend)ist für die Entnahme und den sicheren Transport klinischer Proben mit Viren konzipiert. Es bewahrt die Probenintegrität für nachgelagerte Tests wie zRT-PCR, Viruskultur, UndMolekulare DiagnostikDamit ist es für Krankenhäuser, Labore und öffentliche Gesundheitseinrichtungen weltweit geeignet.

BABIO, zuführender chinesischer HerstellerHersteller von diagnostischen Reagenzien, Transportmedien und Kulturmedien, baut seine Präsenz in weiter ausEuropa, die Vereinigten Staaten, Afrika und Südostasienund bietet vertrauenswürdige Lösungen, die internationalen Standards entsprechen.
Weitere Informationen zu den zertifizierten Produkten und diagnostischen Innovationen von BABIO finden Sie unter: https://www.babiocorp.com
#BABIO #FDA510k #VirusTransportKit #MedicalDevices #Diagnostics #BiotechChina #GlobalHealthcare #ClinicalDiagnostics #Microbiology


